
2. Das Wasserstoffmolekül mit nur einem Elektron:

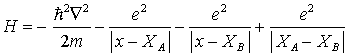
x = Koordinaten des Elektrons
XA = Koordinaten von Kern A
XB = Koordinaten von Kern B


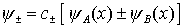
Die Wellenfunktion des Molekülelektrons wird als symmetrische (+) und antisymmetrische (-) Kombination von 1S Wellenfunktionen des H-Atoms angesetzt
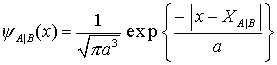

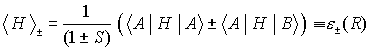

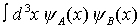

| Energie der Zustände | reine elektronische Energie |
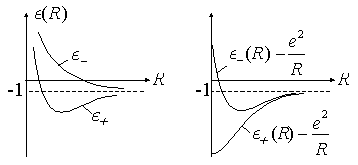
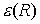 enthält die Coulombabstoßung der Kerne
enthält die Coulombabstoßung der Kerne 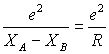

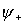 ist bindend, d.h.
ist bindend, d.h.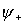 ist zwischen den Kernen größer als
ist zwischen den Kernen größer als 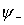 => größere Aufenthaltswahrscheinlichkeit des Elektrons zwischen den Kernen => niedrigere Energie
=> größere Aufenthaltswahrscheinlichkeit des Elektrons zwischen den Kernen => niedrigere Energie 
Quantenmechanik: Teilchen in einem Potentialtopf (qualitativ) Das Wasserstoffmolekül (Wellenfunktionen der Elektronen bei festen Kernen)
Link zum Thema Eintragen - Beitrag zum Thema Schreiben - Persönliche Anmerkung - Diskussionsbeitrag zum Thema

 - mehr Bücher im
- mehr Bücher im