
6. Van der Waals Kraft:

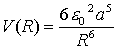 quantenmechanisch
quantenmechanisch 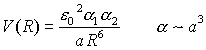 klassisch
klassisch Für Wasserstoffatome im Abstand R
a = Bohrscher Radius
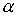 = Polarisierbarkeit
= Polarisierbarkeit 
Wechselwirkung zwischen gegenseitig induzierten Dipolmomenten

Betrachtung des Wechselwirkungsteils des Hamilton Operators des H2 Moleküls als Störung zu den ungestörten Energiezuständen der beiden H Atome =>
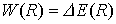 Energieverschiebung der Grundzustandsenergie
Energieverschiebung der Grundzustandsenergie 
Schulphysik: Kraft
Link zum Thema Eintragen - Beitrag zum Thema Schreiben - Persönliche Anmerkung - Diskussionsbeitrag zum Thema


 - mehr Bücher im
- mehr Bücher im