
3. Das Wasserstoffmolekül (Wellenfunktionen der Elektronen bei festen Kernen):

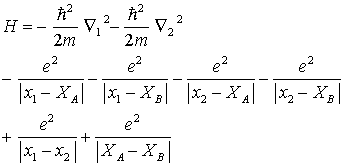

1. Heitler-London Methode: Aufbau der räumlichen Zweiteilchen-Wellenfunktion aus Einteilchen-Wellenfunktionen von isolierten H-Atomen.
2. Methode der Molekülbahnen: Aufbau der räumlichen Zweiteilchen-Wellenfunktion aus Molekülwellenfunktionen des H2+ Moleküls


Singlett-Zustand:

Triplett-Zustand:

Begründung des Ansatzes mit dem Pauli-Prinzip
S(R) = Überlappintegral

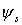 zwischen den Kernen größer ist (
zwischen den Kernen größer ist (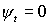 zwischen den Kernen) => energetisch günstigerer Zustand im anziehenden Kernpotential trotz größerer Coulombabstoßung der Elektronen
zwischen den Kernen) => energetisch günstigerer Zustand im anziehenden Kernpotential trotz größerer Coulombabstoßung der Elektronen 
Quantenmechanik: Normierte Wellenfunktionen des Wasserstoffatoms Radiale Wellenfunktionen des Wasserstoffatoms Das Wasserstoffmolekül mit nur einem Elektron
Schulphysik: Austritt von Elektronen aus Leitern
Link zum Thema Eintragen - Beitrag zum Thema Schreiben - Persönliche Anmerkung - Diskussionsbeitrag zum Thema

 - mehr Bücher im
- mehr Bücher im