
5. Kernwellenfuktion beim zweiatomigen Molekül:

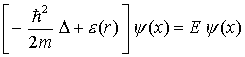
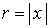
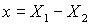 relative Koordinaten der Kerne
relative Koordinaten der Kerne 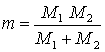 reduzierte Masse
reduzierte Masse 
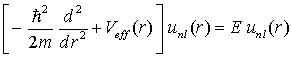
mit dem effektiven Potential:
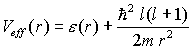

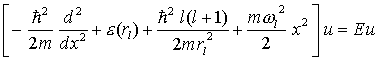

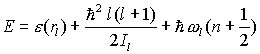

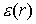 , der Rotations- und der Vibrations(Schwingungs)-Energie zusammen
, der Rotations- und der Vibrations(Schwingungs)-Energie zusammen 

Experimentalphysik 1-4: Kernmitbewegung beim Bohrschen Atommodell
Quantenmechanik: Bestimmung der Energieeigenwerte beim eindimensionalen Potentialtopf Graphische Bestimmung der Bandstruktur beim Kronig Penny Modell Relativistische Massenkorrektur beim Wasserstoff-Atom Feinstrukturaufspaltung beim Wasserstoff-Atom Berücksichtigung der Elektron-Elektron Wechselwirkung beim Helium
Link zum Thema Eintragen - Beitrag zum Thema Schreiben - Persönliche Anmerkung - Diskussionsbeitrag zum Thema

 - mehr Bücher im
- mehr Bücher im